Peptidoglikan hücre duvarının şeker bileşenleri nelerdir?
Peptidoglikan, bakteriyel hücre duvarının temel bileşeni olarak N-asetilglukozamin (NAG) ve N-asetilmüraminik asit (NAM) şeker bileşenlerinden oluşur. Bu yapı, hücre duvarının dayanıklılığını artırarak bakterilerin çevresel koşullara uyum sağlamasına yardımcı olur. Peptidoglikanın işlevleri arasında hücre şeklinin korunması ve antibiyotik direnci bulunur.
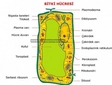
Peptidoglikan Hücre Duvarının Şeker Bileşenleri Nelerdir?Peptidoglikan, bakteriyel hücre duvarının temel bileşenlerinden biri olup, hem yapısal hem de koruyucu bir işlev üstlenmektedir. Bu makalede, peptidoglikanın şeker bileşenleri, bu bileşenlerin yapısı, işlevleri ve bakteriyel hücre duvarındaki rolleri üzerinde durulacaktır. Peptidoglikanın Yapısı Peptidoglikan, iki ana şeker bileşeninden oluşan bir polimerdir: N-asetilglukozamin (NAG) ve N-asetilmüraminik asit (NAM). Bu iki bileşenin tekrarlayan birimlerini içeren bir yapı, hücre duvarının dayanıklılığını ve şekil bozukluğuna karşı direncini sağlamaktadır.
Her hücre duvarı biriminde, NAG ve NAM arasındaki bağlar, β-1,4-glikozidik bağlar olarak adlandırılmaktadır. Bu bağlar, peptidoglikanın uzun, zincirleme yapısını oluşturarak, hücre duvarının sağlamlığını artırmaktadır. Peptidoglikanın Fonksiyonları Peptidoglikanın başlıca işlevleri şunlardır:
Bu işlevler, bakteriyel hücrelerin çevresel koşullara adapte olmasına ve hayatta kalmasına olanak tanımaktadır. Özellikle, antibiyotikler gibi bazı ilaçlar peptidoglikanın yapısına müdahale ederek bakteriyel hücreleri öldürmeyi amaçlamaktadır. Şeker Bileşenlerinin Rolü NAG ve NAM arasındaki bağlar, peptidoglikanın stabilitesini ve dayanıklılığını artırırken, aynı zamanda bakteriyel hücrelerin çevresine karşı koruma sağlamaktadır. Bu şeker bileşenleri, hücre duvarının yapısında yer almanın yanı sıra, bakteriyel virulansın belirlenmesinde de kritik bir rol oynamaktadır.
Bu etkileşimler, bakterilerin konak hücreleriyle iletişim kurmasına ve enfeksiyon süreçlerine katkıda bulunmasına olanak tanımaktadır. Sonuç ve Değerlendirme Peptidoglikan, bakteriyel hücre duvarının temel bir bileşeni olarak, NAG ve NAM gibi şeker bileşenlerine dayanmaktadır. Bu bileşenler, hücre duvarının yapısal bütünlüğünü sağlamanın yanı sıra, bakteriyel hayatta kalma ve virulans süreçlerinde de önemli bir rol oynamaktadır. Bakteriyel enfeksiyonların tedavisinde peptidoglikanın hedeflenmesi, yeni antibiyotiklerin geliştirilmesi açısından önemli bir alan olarak öne çıkmaktadır. Gelecek çalışmalarda, peptidoglikanın daha derinlemesine incelenmesi, bakteriyel hastalıkların tedavisinde yenilikçi yaklaşımlar sunabilir. Bu nedenle, peptidoglikan ve onun şeker bileşenlerinin biyolojik işlevlerinin daha iyi anlaşılması, bilim dünyası için kritik bir öneme sahiptir. |














Peptidoglikan hücre duvarının şeker bileşenleri hakkında bu kadar kapsamlı bir bilgi edinmek gerçekten ilginç. N-asetilglukozamin (NAG) ve N-asetilmüraminik asit (NAM) arasındaki bağlantıların, hücre duvarının dayanıklılığını nasıl artırdığını merak ediyorum. Bu iki bileşenin, bakteriyel hücrelerin çevresel koşullara adapte olmasına nasıl katkıda bulunduğunu daha iyi anlamak, belki de yeni antibiyotiklerin geliştirilmesine ışık tutabilir mi? Ayrıca, peptidoglikan yapısının antibiyotiklere karşı direnç oluşturmadaki rolü gerçekten dikkat çekici. Sizce bu yapıların daha fazla incelenmesi, bakteriyel enfeksiyonların tedavisinde ne gibi yenilikçi yollar açabilir?
Peptidoglikan Hücre Duvarı hakkında gösterdiğin ilgi gerçekten dikkat çekici, Birat. N-asetilglukozamin (NAG) ve N-asetilmüraminik asit (NAM) arasındaki bağların hücre duvarının dayanıklılığını artırma mekanizması oldukça karmaşık. Bu iki bileşen, peptidoglikan yapısının temel birimlerini oluşturur ve birbirleriyle çapraz bağlanarak güçlü bir ağ yapısı oluşturur. Bu yapı, bakteriyel hücrelerin dış etkenlere karşı koruma sağlamasında kritik bir rol oynuyor.
Çevresel Koşullara Adaptasyon açısından, NAG ve NAM, bakterilerin farklı koşullara uyum sağlamasına yardımcı olur. Örneğin, bazı bakteriler, peptidoglikan yapısını değiştirerek osmotik strese, antibiyotiklere veya diğer zararlı maddelere karşı direnç geliştirebilir. Bu adaptasyon yeteneği, bakteriyel enfeksiyonların tedavisini zorlaştıran önemli bir faktördür.
Yeni Antibiyotik Geliştirme bağlamında, bu yapıların daha iyi anlaşılması, antibiyotiklerin etkisini artırma veya direnç geliştiren bakterilere karşı yeni stratejiler geliştirme potansiyeline sahip. Özellikle, peptidoglikan sentezini hedef alan antibiyotiklerin, direnç mekanizmalarını aşmak için yeniden tasarlanması gerekebilir.
Direnç Oluşturma konusuna gelince, peptidoglikan yapısının farklı varyasyonları, bakterilerin antibiyotiklere direnç geliştirmesini kolaylaştırıyor. Bu noktada, araştırmaların bu yapıları ve onların antibiyotiklere karşı sağladığı direnç mekanizmalarını anlamaya yönelik yoğunlaşması, gelecekte bakteriyel enfeksiyonların tedavisinde yenilikçi yollar açabilir. Dolayısıyla, bu alandaki çalışmaların sürekliği, tıpta önemli ilerlemelere yol açma potansiyeline sahip.